氢氧化钠(NaOH)、硫酸镁(MgSO4)、硝酸铅(Pb(NO3)2)、氯化钴(CoCl2)、硫酸镍(NiSO4)、三氯化铁(FeCl3)、硫酸亚铁(FeSO4)、水。
实验步骤:
(1)将氢氧化钠溶于水,配制浓溶液;
(2)将硫酸镁(MgSO4)、硝酸铅(Pb(NO3)2)、氯化钴(CoCl2)、硫酸镍(NiSO4)、三氯化铁(FeCl3)、硫酸亚铁(FeSO4)溶于水,配制浓溶液;
(3)向水中倒入氢氧化钠浓溶液,使用玻璃棒搅匀,向其中滴加(2)中溶液,产生各色沉淀,并沉入容器底部。
实验原理:
在初高中的化学知识体系里,对于金属的氢氧化物,一般认为只有氢氧化钾(KOH)、氢氧化钠(NaOH)和氢氧化钡(Ba(OH)2)是溶于水的,氢氧化钙(Ca(OH)2)是微溶于水的。实际上碱金属的氢氧化物都是溶于水的,并且阴阳离子半径相差较大的离子化合物在水中的溶解度较大,这个规律也适用于碱土金属的氢氧化物。
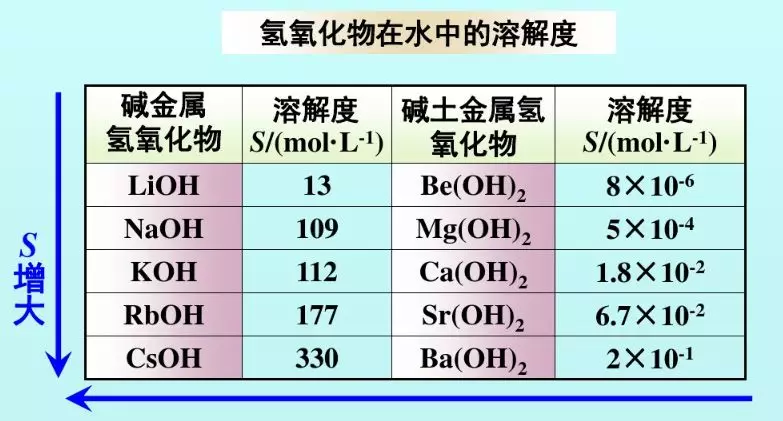
而在视频中的金属氢氧化物都是难溶于水的,所以会形成各色沉淀。
化学反应方程式分别为:
CuSO4+2NaOH=Na2SO4+Cu(OH)2
MgSO4+2NaOH=Na2SO4+Mg(OH)2
Pb(NO3)2+2NaOH=2NaNO3+Pb(OH)2
CoCl2+2NaOH=2NaCl+Co(OH)2
NiSO4+2NaOH=Na2SO4+Ni(OH)2
FeCl3+3NaOH=3NaCl+Fe(OH)3
FeSO4+2NaOH=Na2SO4+Fe(OH)2
复杂等级
危险等级
温馨提示:
重金属盐的氢氧化物沉淀是有毒并且会污染环境!
请不要在家中进行此实验!
在实验室需将废液妥善处理!